Медицинский стартап — это не просто технология, а обязательство перед врачами и пациентами. О том, как провести аналог клинических испытаний для своей идеи, реальных ошибках и фазах, которые помогут проверить, что продукт нужен рынку, рассказывают Ксения Алексеева, СЕО коммуникационного агентства Fresh Russian Communications, и Наталья Архипова, руководитель направления аналитики агентства FRC.
Чем проверка спроса на стартап похожа на клиническое испытание лекарства
Мир медицинских технологий полон блестящих идей, которые так и не дошли до пациентов. Причем провалы случаются не только с лекарствами, но и со стартапами. Самый известный пример — Theranos. Компания обещала революцию: сотни анализов из капли крови. В проект инвестировали сотни миллионов долларов, им восхищались СМИ и инвесторы. Но технологию так и не смогли подтвердить клинически: результаты тестов оказались недостоверными, проект рухнул. В 2018 году компания была ликвидирована, а её основатели обвинены в мошенничестве*.
Theranos — лишь громкий пример проблем с самим продуктом. На практике многие медицинские стартапы терпят поражение по менее драматичным причинам: строят решение без проверки реальной боли врачей, не тестируют MVP на целевой аудитории, запускают пилот без фиксированных целей. Такие действия противоречат устоявшемуся в медицине порядку, где прежде чем выпустить новое лекарство на рынок, обязательно проводят клинические испытания — многоступенчатый процесс, где каждое решение проверяется фактами. А в стартапах часто пытаются «выписать рецепт» рынку, не убедившись, что диагноз поставлен верно.
Поэтому мы предлагаем методологию проверки спроса, оформленную как 4 фазы клинических испытаний. Использование именно этой метафоры будет полезно, потому что:
● ваши будущие клиенты — врачи и администраторы клиник — привыкли мыслить в терминах «фазы испытаний»;
● «валидация» в стартапе так же важна, как клиническое доказательство для лекарства;
● системный подход снижает риск потратить годы и инвестиции на заведомо провальное решение.
Давайте разберём, как пройти все «фазы испытаний» вашего стартапа — от безопасной гипотезы до работающего пилота.
Фаза 0. Доклинический этап: безопасность гипотезы
Прежде чем тестировать лекарство, его проверяют на безопасность. То же самое нужно сделать и со стартапом: убедиться, что гипотеза «не токсична» — не слишком размыта, не требует догадок, не строится на предположениях.
Частая ошибка основателей — начинать с лозунга «хочу внедрить вот это, чтобы улучшить медицину». Но улучшить можно что угодно и для кого угодно, а во внедрении вашей идеи пока заинтересованы только вы. Важно сузить фокус до конкретной аудитории и проблемы, которую можно измерить. Для этого воспользуйтесь следующей последовательностью действий (пример приведен на основе вымышленной компании N, развивающей платформу прогнозной медицинской аналитики):
Шаг 1. Подробно опишите, кто ваш пациент (целевая аудитория)
Пример: Целевая аудитория (ЦА) у такого стартапа может быть изначально из сектора государственного здравоохранения: руководители медицинских организаций и государственных органов в этой сфере, врачи, работающие с электронными медицинскими картами (ЭМК), специалисты диспансеризации и контроля качества в регионах. Поэтому при выходе на рынок ЦА для этого продукта может быть сформулирована как «региональные административные органы здравоохранения (например, департаменты/минздравы), ответственные за популяционный мониторинг и диспансеризацию, которые имеют ЭМК-системы и заинтересованы в снижении числа осложнений хронических заболеваний». Обратите внимание, что чем детальней описание, тем проще вам будет искать свою ЦА для прохождения следующих фаз и формулировать для них ценность вашего предложения.
Шаг 2. Поставьте диагноз (сформулируйте проблему и вызовы отрасли)
Пример: ЭМК содержат неструктурированные данные, большую часть информации сложно автоматизировать и анализировать, отсутствуют инструменты, которые автоматически выявляют группы риска, контролируют качественные метрики и предупреждают осложнения (например, хронические болезни, сердечно-сосудистые заболевания). ЦА же остро нуждается в такой прогнозной аналитике и автоматизации, которые помогли бы ей в работе.
Шаг 3. Предложите лечение (своё решение)
Пример: Гипотеза-решение данного MedTech-стартапа могла выглядеть так: «Платформа на основе ИИ, интегрируемая с ЭМК, которая автоматически обрабатывает обезличенные данные, извлекает факторы риска, статистику по пациентам и региону, генерирует прогнозы и рекомендации для врачей и руководства, позволяя своевременно выявлять группы риска и корректировать стратегию оказания медицинской помощи населению». Имейте ввиду, что на первом этапе не нужно описывать ваш продукт в деталях. Это пока гипотеза, а не финальный прототип.
Шаг 4. Дайте прогноз (эффект, ценность внедрения решения)
Пример: «Внедрение продукта N приведёт к сокращению числа осложнений и госпитализаций за счёт раннего выявления групп риска, улучшится качество диспансеризации, снизится процент ручной работы врачей по анализу данных и повысится достоверность и своевременность их вмешательства». Создатели продукта могут заявить и том, что эффектом для ЦА станет экономия бюджетных средств здравоохранения, повышение эффективности распределения ресурсов. Однако тут будьте бдительны: такие выражения должны быть подтверждены вашими внутренними расчётами, то есть конкретными цифрами и фактами.

После того, как вы составили данную схему, смело переходите к следующей фазе «испытаний».
Фаза I. Проверка на небольшой группе добровольцев
Когда лекарство проходит доклинический этап, его начинают тестировать на небольшой группе пациентов — чтобы убедиться, что эффект действительно есть. В стартапе этот этап соответствует проверке того, существует ли проблема, которую вы хотите решать, и насколько она болезненна для вашей целевой аудитории.
Например, российский стартап в сфере телемедицины Polyclinica** одним из первых попытался решить, как они считали, очевидную проблему — пользователи не знают, к какому врачу обращаться по симптомам. Основатели разработали MVP, участвовали в конференциях и промо, но в итоге поняли, что спрос и мотивация целевой аудитории значительно слабее, чем они думали. В результате гипотеза не подтвердилась, и проект был заморожен на стадии MVP. Пропустив вторую фазу оценки спроса, команда упустила возможность стать лидером резко выросшего в последующие годы рынка телемедицины. Проведение 15-20 качественных чётко структурированных интервью могло бы помочь проекту увидеть реальную боль пользователей и скорректировать свою идею.
Как действовать в этой фазе:
Шаг 1. Определите цель проверки
Вам важно не просто «понять, есть ли интерес», а сформулировать измеримые вопросы: «Как часто врачи сталкиваются с этой проблемой?», «Как сильно она влияет на их работу или доход?», «Какие решения они уже пробовали?», «Кто принимает решение о внедрении инноваций, кто на этот процесс влияет, а кто внедрённым решением пользуется?»
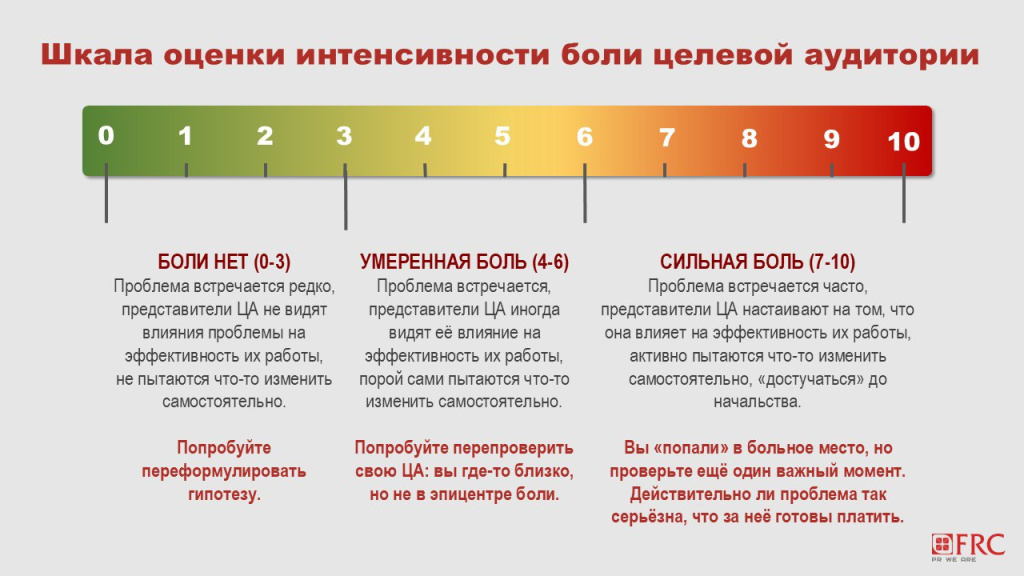
Результат должен быть количественно выражен: Например, если 70% врачей признают, что ежедневно тратят на ручной ввод данных больше 30 минут — боль существует. Если 2 из 20 сказали «бывает иногда» — нет.
Шаг 2. Проведите 15–20 глубинных интервью
Интервью — это не анкетирование, а диагностический осмотр. Ваша задача — понять симптомы, а не подтвердить диагноз. Задавайте открытые вопросы и внимательно слушайте развёрнутые ответы: «Что раздражает в текущем процессе?», «Что вы уже пробовали, чтобы исправить это?», «Что произойдет, если ничего не менять?» Остерегайтесь закрытых формулировок вроде «Вам было бы полезно наше решение?» Это как спрашивать пациента: «Вы хотите чувствовать себя лучше?» — ответ очевиден, но для дела бесполезен.
Шаг 3. Фиксируйте язык боли
Когда человек говорит о настоящей проблеме, он использует эмоциональные слова: «ненавижу», «надоело», «каждый день», «опять эти таблицы». Если вместо этого вы слышите: «ну, бывает», «да, неудобно, но терпимо» — явной проблемы нет.
Фаза II. Оценка рынка и сравнение с «контрольной группой»
После того как действие нового лекарства на организм нескольких здоровых добровольцев изучено, наступает момент первого столкновения с внешним миром.
Это этап, где стартап впервые выходит за пределы «стерильной среды» — своих презентаций и интервью — и проверяет: а есть ли на рынке место для такого лекарства вообще? В клинических испытаниях на этой фазе препарат вводят пациентам с заболеванием, чтобы оценить эффективность препарата и определить оптимальный режим дозирования. В нашем случае «пациентами» становятся инвесторы, дистрибьюторы, IT-директора и администраторы клиник, которые не страдают болью напрямую, но хорошо понимают контекст отрасли и трендов.
Что проверяется на этом этапе:
● Сегмент и платёжеспособность. Кто готов платить — государство, частная медицина, пациент? Каков путь будущей сделки: кто принимает решение на каждом из этапов?
● Размер рынка. Сколько клиник, врачей или страховых компаний потенциально могут использовать продукт?
● Конкуренция. Какие «аналоговые лекарства» уже существуют — и почему ими недовольны?
● Барьеры входа. Требуется ли регистрация как медизделия, сертификация по 152-ФЗ, совместимость с МИС?
Как проводить «испытания» в рамках данной фазы:
Шаг 1. Начните с кабинетных исследований потенциала рынка
Начинать оценку потенциала рынка советуем по методу «снизу вверх» — с описания и расчёта тех сегментов, которые вы реально можете охватить. Разбейте рынок на конкретные группы: по типу клиники (частная, государственная), специализации врачей, количеству пациентов в день, региону или типу услуг. Оцените, сколько клиник и врачей из каждого сегмента вы реально сможете привлечь в первые 12–24 месяца. Такой подход позволяет получить реалистичную внутреннюю оценку доли рынка, до которой вы действительно сможете дотянуться, и планировать пилотные проекты, продажи, штат команды, бюджет на маркетинг и PR без иллюзий.
После этого будет удобно представить данные в формате классической модели PAM/TAM/SAM/SOM «сверху вниз», к которой уже привыкло бизнес-сообщество:
● PAM (Potential Available Market) — потенциально доступный рынок, то есть максимальный спрос на продукт или услугу.
● TAM (Total Addressable Market) — общий объем рынка, то есть рынок, на котором продукт может быть фактически продан.
● SAM (Serviceable Available Market) — обслуживаемый доступный рынок, или та часть рынка, на которую ваш стартап нацелен и которую он может обслужить.
● SOM (Serviceable Obtainable Market) — доля, которую вы реально сможете занять в первые годы работы (если вы заранее провели оценку по методу «снизу вверх», то подсчитать эту долю будет намного проще, чем гадать на кофейной гуще, оценивая проценты: 0,5%? Или 1%? А вдруг сможем взять сразу 3,6%?)
Модель полезна для визуализации масштаба рынка и демонстрации инвесторам потенциала, но для внутренних решений важнее ориентироваться на реалистичные сегменты и достижимую долю, а не на абстрактные глобальные цифры.
Шаг 2. Проведите конкурентный анализ
Выясните, кто уже решает ту же проблему, которую вы собираетесь лечить. Разделите конкурентов на прямых (те, кто предлагает продукт с такой же функциональностью), косвенных (альтернативные способы решения проблемы, например ручные процессы или другие сервисы) и неформальных («как делают сейчас», обходные пути). Оцените их сильные и слабые стороны: что у них работает, что вызывает недовольство пользователей, где есть пробелы, которые может заполнить ваш продукт.
Кроме того, не забывайте про ценностное предложение конкурентов: насколько оно реально сокращает боль пользователя, а не является маркетинговой формулой. Для визуализации удобно собрать сравнительную таблицу с основными характеристиками конкурентов и добавить цветовое кодирование — зелёным отмечаете сильные стороны, красным — слабые. Такой анализ помогает увидеть, где ваш стартап может реально «вылечить болезнь», а где его шансы невелики.
Шаг 3. Соберите панель отраслевых экспертов.
Врачи, главврачи, инвесторы, представители Минздрава или медицинских ИТ-компаний. Пусть они «пробуют препарат на вкус» — оценивают идею с точки зрения опыта и регуляторных рисков. Здесь рождаются самые ценные инсайты: иногда выясняется, что продукт нарушает нормативы, требует дорогостоящей сертификации или дублирует функции существующих решений.
Шаг 4. Сформируйте вывод о «токсичности».
Если исследования показывают, что конкуренты уже сильно вас опережают и уже решают проблему (а ваше решение ничем не лучше), или больше половины экспертов считают, что продукт «нежизнеспособен» из-за регулирования или отсутствия спроса — значит, препарат не стоит выводить в следующую фазу.
Обратите внимание, что эта фаза важна не только для вашего внутреннего понимания, но и для ваших помощников на пути к коммерциализации: например, для получения статуса резидента «Сколково» (сегодня для многих MedTech-компаний это ключ к инфраструктуре, налоговым льготам и доступу к инвесторам, готовым поддерживать высокорисковые технологические проекты). Однако, чтобы получить этот статус, заявка должна убедительно показать, что проект не только научно интересен, но и коммерчески жизнеспособен.
Наше агентство как-то консультировало команду одного стартапа, которая на первом этапе как раз столкнулась с отказом экспертной комиссии «Сколково». Их продукт был перспективным — действительно помогал избавить целевую аудиторию от «боли» — но заявка не содержала качественной оценки рынка: ни данных о размере сегмента, ни анализов конкурентов, ни понимания, кто именно будет принимать решение о закупке продукта в клиниках. Эксперты отметили, что без подтверждения спроса проект выглядит больше как исследовательский, а не коммерческий. После доработки заявки — проведённых интервью с врачами и администраторами, уточнения целевых сегментов и расчёта потенциала рынка по обеим моделям «снизу вверх» и PAM/TAM/SAM/SOM — проект получил одобрение и статус резидента. Этот кейс хорошо показывает, что для стартапа важна не только технология, но и доказательная база того, что рынок действительно ждёт ваше решение.

Фаза III. Испытание прототипа: проверяем, работает ли решение
Когда гипотеза подтверждена, а боль целевой аудитории доказана, пора переходить к следующему шагу — тесту самого решения. В медицине это фаза, когда исследователи вводят препарат большой группе пациентам с заболеванием, чтобы увидеть, действует ли он в реальных условиях. В стартапе аналогом станет проверка MVP — минимально жизнеспособной версии продукта. На этом этапе основателю важно не тратить месяцы на разработку, а быстро создать «модель лекарства» — прототип, который позволит проверить, работает ли формула.
Для MedTech-продукта это может быть:
● короткое демо-видео (2–3 минуты);
● интерактивный макет в PowerPoin/Figma;
● краш-тест на открытых данных (для ИИ-решений);
● имитация интерфейса на бумаге — если этого достаточно, чтобы получить требуемую реакцию пользователей.
Главная цель фазы III — не убедить всех, что идея прекрасна, а проверить, купят ли люди «таблетку», когда она ещё не покрыта оболочкой (маркетинговыми решениями).
Как грамотно проводить испытание MVP:
Шаг 1. Покажите прототип тем, кто подтвердил боль.
Тестировать решение следует именно на тех, кто ранее жаловался на проблему, иначе вы получите искажённую обратную связь.
Шаг 2. Наблюдайте за реакцией, а не за словами.
Если пользователь интересуется ценой или просит показать функционал — это признак интереса. Если говорит «прикольно, но…» — это отказ. И здесь речь не о том, что некоторые люди сами по себе консерваторы и противятся изменениям. Вы, скорее всего, не раз услышите что-то вроде: «Ой, придётся разбираться в новой программе/устройстве, это же займёт много времени!». Да, любое изменение требует изначального вложения сил и концентрации. Постарайтесь услышать реакцию на эффект, который ожидается после внедрения решения. Согласен ли респондент с тем, что результат стоит потраченных усилий?
Шаг 3. Задайте ключевой вопрос:
«Если бы это работало уже сегодня, вы бы стали использовать?»
Шаг 4. Соберите данные для анализа.
Подсчитайте, сколько людей захотели попробовать, сколько готовы платить и/или стать инфлюенсером (проталкивать ваш продукт в системе медицинской организации), какие сомнения возникли. На основе этого можно рассчитать ранний показатель «лечебного эффекта» — коэффициент валидации (например, 30% опрошенных готовы к пилоту).
Фаза IV. Внедрение и масштабирование (пилот и постмаркетинговые исследования)
На этом этапе лекарство уже доказало свою эффективность в контролируемых условиях, но теперь его действие проверяют после начала использования, «в полях» — среди реальных пациентов, с разными диагнозами и контекстами. Для стартапа этот этап аналогичен выходу в реальную клиническую среду: когда прототип превращается в работающий инструмент, а команда получает живые данные о его пользе и ограничениях. Главная цель — не просто показать, что технология работает, а собрать доказательства, которые убедят рынок, инвесторов и регуляторов, что решение уже приносит измеримую пользу.
Шаг 1. Найдите пилотного партнёра.
Наиболее удачные пилоты проходят там, где есть «чемпион» — врач, администратор или ИТ-специалист, заинтересованный в решении вашей проблемы. Он поможет внедрить продукт, объяснить коллегам, зачем он нужен, и удержать внимание команды до конца тестирования.
Шаг 2. Определите цели.
Как и в клинических исследованиях, измеримость — ключ к доверию. Установите конкретные метрики: «сократить время приёма на 30%», «повысить точность диагностики на 15%», «уменьшить количество ошибок в документации в 2 раза». Без чисел результат пилота невозможно защитить перед инвесторами и новыми клиентами.
Шаг 3. Зафиксируйте договорённости.
Пилот — это не дружеский эксперимент, а управляемый проект. Подписывайте NDA и договор, прописывайте сроки, роли и права на результаты. Без этого вы рискуете потерять контроль над данными и, как следствие, над самой историей успеха.
Шаг 4. Сравните данные «до и после».
Это ваш главный актив. Фиксируйте стартовые показатели, собирайте обратную связь во время пилота, а затем представьте изменения — визуально, в цифрах, в цитатах пользователей. Даже небольшой, но подтверждённый результат может стать пропуском к масштабированию и новым партнёрствам.
Шаг 5. Обеспечьте PR-поддержку пилота.
Во время пилотного запуска продукта важно не ограничиваться техническими испытаниями – PR-поддержка проекта. Публикации о ходе пилота и первых результатах повышают доверие к стартапу и продукту. Внешние коммуникации формируют репутацию и демонстрируют реальную пользу: когда о стартапе пишут в авторитетных СМИ, у потенциальных пациентов, врачей и инвесторов складывается впечатление, что ему можно доверять. Практика МедТех-стартапов показывает, что решения с сильным медийным присутствием привлекают капитал быстрее (например, биотех-стартапы с хорошим PR получают инвестиции в 2,3 раза быстрее***).
Нина Матвиенко, директор департамента продуктового маркетинга команды Big Data & AI Билайна подтверждает, что в медицине доверие формируется через открытость и постоянное общение с профессионалами: “Поэтому рассказывать о собственных medtech-разработках важно регулярно и начинать еще на ранних этапах. Например, мы вместе с командой Сеченовского университета в рамках совместного предприятия «МедТех ИИ» разрабатываем решения на базе ИИ для медицины, в частности для цифровой патоморфологии. Наш PR строится на постоянном освещении проектов, научных публикациях и диалоге с медсообществом и госструктурами, что помогает не только информировать рынок, но и привлекать партнеров. Ранний PR — это не просто промо, а важный канал для привлечения врачей и экспертов, с которыми мы обсуждаем результаты пилотов, обмениваемся опытом и развиваем технологии. Так мы усиливаем позиции и убедительность наших решений на рынке”.
“PR-поддержка — необходимый блок развития стартапа. Сложно переоценить важность цифрового следа в виде публикаций в медиапространстве, поскольку регулярные упоминания позволяют людям запомнить вас, а регулярные рассказы о достижениях и ведении проекта формируют доверие. Может быть и так, что у стартапа есть поддержка крупного бренда, ей обязательно нужно пользоваться, потому что так вы можете усилить друг друга . У нас так, например, получилось с «Фенистилом» и нашим сервисом Checkderm, который выявляет дерматологические проблемы по фото кожи. Благодаря сервису мы смогли повысить узнаваемость бренда «Фенистил», одновременно повысив доверие и к нашим разработкам. Аналогично с брендом «Магнит косметик» и сервисом Beautyscan”, — рассказывает Евгений Соболев, сооснователь российско-корейской биотех студии Scanderm.
Но каждый случай индивидуален и требует тщательного планирования PR-активности, иногда существенно расширяя поле работы. Например, российская компания Medgital, которая занимается разработкой навигационных систем для хирургии на основе технологий дополненной реальности, прошла все основные вехи “дороги в Изумрудный город”, поделился с нами генеральный директор компании Владимир Иванов. Medgital стала резидентом “Сколково”, выступала на всех ведущих телеканалах, навигационная система Medgital Vision получила регистрационное удостоверение на медицинское изделие, сама система проходила пилотирование в 14 ведущих медицинских центрах России, а генеральный директор выступал перед министрами и в Госдуме. Компанией были получены гранты от Сколково, ФСИ, РНФ, опубликованы статьи в ведущих научных журналах уровня Скопус Q1.
«Казалось бы, вся программа PR была выполнена и перевыполнена. Но продажи продолжали оставаться единичными. А при общении с инвесторами этот показатель имеет решающее значение: «Вот когда у вас будут сотни продаж, тогда и приходите». Справедливости ради следует отметить, что при цене продажи изделия порядка 10 млн руб, выход на сотни продаж означает, что инвестор и не нужен», — рассказывает Владимир Иванов.
Исправить ситуацию компании помогли несколько факторов. Во-первых, это присутствие в сетях профессионального сообщества, например, в Телеграм-каналах сообществ. «Там надо находиться, выкладывать результаты, реагировать на критику и на восторженные отклики. Это лучшая обратная связь, через которую вы получите информацию о необходимых улучшениях вашего продукта, а кроме того, через эти сети придут и новые заказчики», — делится Владимир Иванов.
Второе — это выход на зарубежные рынки. Появление первых продаж в Индии, Мексике и Эквадоре и победы в престижных международных конкурсах стартапов, в частности, в китайском HICOOL в Пекине были весьма кстати.
Наконец, это переформатирование ситуации. «Классическим примером подобного подхода является поиск денег С.П.Королевым на космический проект. Только тезис, что это еще и укрепит оборону страны, дал требуемый результат. Поэтому и в нашем случае возможность внедрения разработанных медицинских технологий в такие области, как образование, ветеринария, телемедицина, медицина катастроф, корабельная и арктическая медицина, также служит нужным подспорьем», — говорит Владимир Иванов.

Заключение: побочные эффекты успеха и как их контролировать
Как и в клинической практике, даже после выхода лекарства на рынок продолжается наблюдение за его безопасностью и эффективностью. Для стартапа это означает, что работа над продуктом не заканчивается после пилота — наоборот, начинается этап постоянного улучшения на основе данных, обратной связи и реальных сценариев использования.
Каким бы сложным ни выглядел описанный выше процесс валидации, помните, что он не про интуицию и вдохновение, а про научный подход и доказательства. Пройдя все четыре фазы — от лабораторной идеи до масштабирования в реальной клинической среде, — вы получите не просто прототип, а зрелое решение с подтверждённой ценностью, которому доверяют и пользователи, и рынок.
Начните с малого — сформулируйте гипотезу, оформите её как медицинскую «карту» проекта и обсудите с врачами. Именно с этого шага начинается путь стартапа, способного пройти собственные «клинические испытания» и стать по-настоящему востребованным в здравоохранении.
*Источник: https://www.sostav.ru/publication/skandalnyj-startap-theranos-prekratit-sushchestvovanie-33194.html
** Источник: https://habr.com/ru/articles/550626/
Следите за нашими новостями в Telegram-канале FreshPR















